مشهورترین باتریهای موجود در بازار، باتریهای سرب اسید، نیکل کادمیوم(معروف به نیکاد Ni-Cd) نیکل متال هیدرید(Ni-MH) و باتریهای لیتیم یون هستند که باتریهای لیتیم یون نیز انواع مختلفی دارند. مصرف بالای سوخت های فسیلی و افزایش تقاضای انرژی باعث شده است که تجسس و تحقیقات جهانی در خصوص مواد و ابزار ذخیره سازی انرژی افزایش یابد. از این رو توسعه سریع ابزارهای الکترونیکی مدرن منجر به افزایش تحقیق در خصوص موادی که دارای توانایی بالایی جهت ذخیره انرژی بالایی هستند، این ابزارها نقش مهمی در نسل جدید و قابل بازیافت سیستم های انرژی دارند.
1- باتری سرب اسید:
باتری اسیدی یا باتری سربی اسیدی گونهای از باتری قابل شارژ است که در سال 1859 توسط فیزیکدان فرانسوی، گاستون پلانته اختراع شد. علی رغم ذخیرهی کم انرژی نسبت به وزن و حجم آن، به دلیل هزینهی پایین و عرضهی زیاد، در وسایل نقلیه موتوری به تعداد بسیار زیاد مورد استفاده قرار گرفت. بهطور کلی اختلاف ولتاژ ایجاد شده به کمک یک سلول از الکترودهای مثبت و منفی در باتری های سرب اسیدی حدود ۲ تا 1/2 ولت است؛ لذا ولتاژهای بالاتر مثل ۱۲ ولت از اتصال سری چندین سری از الکترودهای مثبت و منفی تشکیل میشود. قطر صفحات مثبت و منفی نقش اساسی در تعیین ظرفیت باتری بازی میکنند. اغلب برای کاربردهای با ظرفیت معمول همچون باتری های استارتر خودرو، قطر این صفحات کمتر از ۲ میلیمتر است.

مزایای باتری سرب اسید:
معایب باتری سرب اسید:
کاربرد باتری سرب اسید:
2- باتری نیکل کادمیوم:
باتریهای نیکل کادمیوم گونهای از باتریهای قابل شارژ هستند که در آن از نیکل (III) اکسید و کادمیوم به صورت فلز به عنوان الکترود استفاده شده است. این نوع از باتریها نخستین بار توسط مهندس سوئدی والدمار جانگنر در سال 1899 میلادی اختراع گردید. مصرف عمدهی این نوع از باتریها در لوازم الکترونیکی چون گوشیهای تلفن همراه است . در مقایسه با سایر باتری های قابل شارژ، باتری های نیکاد (نیکل کادمیوم)، دارای چرخه کار بهتری هستند اما مهم ترین مزیت آنها تحویل ظرفیت نامی حتی در نرخ دشارژ بالا است اگرچه، این باتری ها دارای قیمت بالاتری نسبت به باتری های سرب اسید هستند و نرخ خود دشارژی این باتریها بالاست.

مزایا باتری نیکل کادمیوم:
معایب باتری نیکل کادمیوم:
کاربرد باتری نیکل کادمیوم:
3- باتری نیکل متال هیدرید:
باتری نیکل متال هیدرید، نخستین بار در سال ۱۹۸۹ میلادی به صورت تجاری به بازار عرضه شدند. این باتریها شباهت زیادی به نوع نیکل کادمیوم دارند که در این باتری الکترود مثبت از جنس نیکل اکسید (مانند باتریهای نیکل-کادمیومی) و الکترود منفی از جنس آلیاژ جذب کننده هیدروژن (به جای کادمیوم) است. باتریهای Ni-MH (یا همان باتری نیکل متال هیدرید) دارای سی تا چهل درصد قابلیت انبار بیشتر نسبت به معادل های نیکل کادمیوم هستند، اما تعداد چرخه شارژ و دشارژ کمتری را پشتیبانی می کنند که به طور معمول بین ۳۰۰ تا ۵۰۰ چرخه است. این باتری دارای ظرفیت جریان دهی بیشتر، مقاومت داخلی کمتر و چگالی حجمی و جرمی بیشتری است و این مدل باتریها در دوربین های عکس برداری کابرد زیادی دارند.
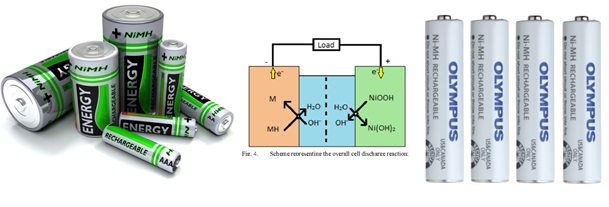
مزایای باتری نیکل متال هیدرید:
معایب باتری نیکل متال هیدرید:
کاربرد باتری نیکل متال هیدرید:
4- باتریهای لیتیم یونی:
باتری های لیتیومی به میزان زیادی در وسایل الکترونیکی و خودروهای هیبریدی برقی استفاده شده است و در ایتدا بکارگیری این باتری ها توسط شرکت سونی بطور موفقیت آمیزی در سطح اقتصادی صورت گرفت. اما به دلیل کمیاب بودن و قیمت بالای لیتیوم کاربردهای بیشتر این ماده در سیستم های ذخیره انرژی در ابعاد بزرگ اقتصادی محدود شده است. بنابراین یافتن مواد جدید و جایگزین لیتیوم بسیار حائز اهمیت است.
استراتژی های کلی جهت بهبود عملکرد الکتروشیمیایی سلنیدهای فلزی شامل سنتز ساختارهایی در ابعاد نانو و بکارگیری مواد کربن اسئوس carbonaceous است. هدف کلی این استراتژی ها بهبود عملکرد الکتروشیمیایی از طریق افزایش خصوصیات سنتیکی سلنیدهای فلزی است. ولی مشکل افزایش حجم و جریان پایین الکترون سلنیدهای فلزی در زمان چرخش یا جریان الکترون را میتوان با استفاده از ترکیب با گرافن بهبود داد. زمانیکه گرافن به درون سیستم های الکترودی وارد می شود مواد کامپوزیت آندی سلنیدهای گرافن/فلز بطور طبیعی منجر به شکل گیری اینترفیس (G/Na2Se (G/NSe در زمان بدون شارژ می شوند.
موادی که اساس کربنی دارند نقشی زیادی در ذخیره انرژی در باتری های لیتیومی خواهند داشت. مواد برگرفته از گرافیت بطور خاصی جهت استفاده در ابزارهای ذخیره انرژی بخصوص باتری های لیتومی مناسب هستند و این قابلیت آنها به دلیل ساختار لایه ای و واکنش برگشت پذیر بین این مواد و ترکیبات لیتیوم-کربنی است، که بعنوان الکترولیت استفاده می شود. گرافیت به میزان بالایی بعنوان مواد آندی در ساختار باتری های لیتومی استفاده می شود و استفاده بالای این ماده در ساختار این باتری ها به دلیل خصوصیات الکتروشیمیایی و فیزیکی منحصر به فرد این ماده است.
گرافن که ماده ای دو بعدی برپایه کربن است در سال 2004 توجه محققین که در خصوص باتری های لیتیومی تحقیق می کردند، به خود جلب نمود. دلیل این امر ضخامت اتمی، خصوصیات الکترونیکی ویژه و قدرت مکانیکی بالا، انتقال دمایی بالا و نسبت سطح به حجم خیلی بالای آن است. گرافن اکسید را می تواند به راحتی در حجم خیلی بالایی از طریق اکسیداسیون شیمیایی و لایه برداری گرافیت تولید می شود.
گرافن به دو روش کلی از بالا به پایین (Top-down) و از پایین به بالا (Bottom-up) تولید می شود. بطوریکه در روش بالا به پایین از منابع گرافیتی کربنی استفاده می شود. این مواد گرافیتی از طریق لایه برداری مکانیکی، لایه برداری شیمیایی/الکتروشیمیایی فاز مایع یا بازکردن نانولوله های کربنی تولید می شوند. اما در روش از پایین به بالا، از منابع کربنی غیر گرافیتی استفاده می شود.
جهت کاهش و لایه برداری اکسید گرافن و اکسید گرافیت روش هایی همچون کاهش شیمیایی، کاهش دمایی، کاهش میکروویو و کاهش لیزری استفاده می شود. گرافن یا گرافن اکسید که برای ذخیره انرژی در باتری های لیتیومی استفاده می شود هم بعنوان آند و هم بعنوان کاتد می توانند استفاده شوند. موادی که بر پایه گرافن یا گرافن اکسید هستند و بعنوان آند استفاده می شوند شامل موارد زیر است:
1- گرافن/گرافن اکسید با اکسیدهای فلزی،
2- گرافن/گرافن اکسید با مخلوطی از اکسیدهای فلزی،
3- گرافن/گرافن اکسیدهایی با سولفیدهای فلزی یا مخلوطی از سولفیدهای فلزی،
4- گرافن/گرافن اکسید دوپ شده با اکسیدهای فلزی یا مخلوطی از اکسیدهای فلزی،
5- گرافن/گرافن اکسید دوپ شده با سولفیدهای فلزی،
6- نانوکامپوزیت های گرافن/سلیس
باتری لیتیم یون(LiB) خانوادهای از باتریهای قابل شارژ است که در زمان تخلیه، یونهای لیتیم از سمت الکترود منفی به سمت الکترود مثبت و در هنگام شارژ شدن از سمت از سمت الکترود مثبت به سمت الکترود منفی حرکت میکنند. باتریهای لیتیم یون بالاترین چگالی انرژی را فراهم میسازند که تقریباً دو برابر انرژی قابل دسترسی از باتریهای نیکل کادمیوم است. باتریهای لیتیم یون معمولاً برای تأمین انرژی لازم در دستگاههای الکترونیکی قابل حمل مورد استفاده قرار میگیرند. در مقایسه با نسلهای قدیمیتر باتریها یعنی باتری نیکل کادمیوم و باتری نیکل هیدرید فلز، باتریهای لیتیم یون وزن و حجم سبکتری در حدود ۳ تا ۵ برابر دارند و در هنگام دشارژ افت ولتاژ کمی از خود نشان میدهند. باتری لیتیم یون انرژی زیادی تولید میکند اما در مقابله با باتریهای نیکل هیدرید، ایمنی آنها پایین است. برای نمونه، این نوع باتریها زود آتش میگیرند اما نسل جدید باتری لیتیم یون با حل مشکلات خود، هر نیازی را براورده میکنند. آنها به دشارژ کامل نیاز ندارند و میتوان از جریان الکتریکی بالاتر برای شارژ و دشارژ از آنها بدون آسیب به باتری استفاده کرد. یک باتری لیتیم یون را میتوان در هر زمانی بدون آنکه روی کارایی باتری اثر گذارد، شارژ نمود. اما به دلیل این که باتریهای لیتیم یون دارای طول عمر معمول شارژ و دشارژ ۳۰۰ تا ۵۰۰ چرخه هستند، اگر زود به زود و قبل از تخلیه، شارژ شوند طول عمر باتری پایین میآید. همچنین در این باتریها در صورت ادامه شارژ پس از پر شدن، باتری آسیب دیده و از عمر آن کاسته میشود به همین دلیل برای شارژ آنها از مدارهای محافظ هوشمند استفاده میشود تا پس از کامل شدن فرایند شارژ، جریان قطع شده و باتری بیش از حد شارژ نگردد.
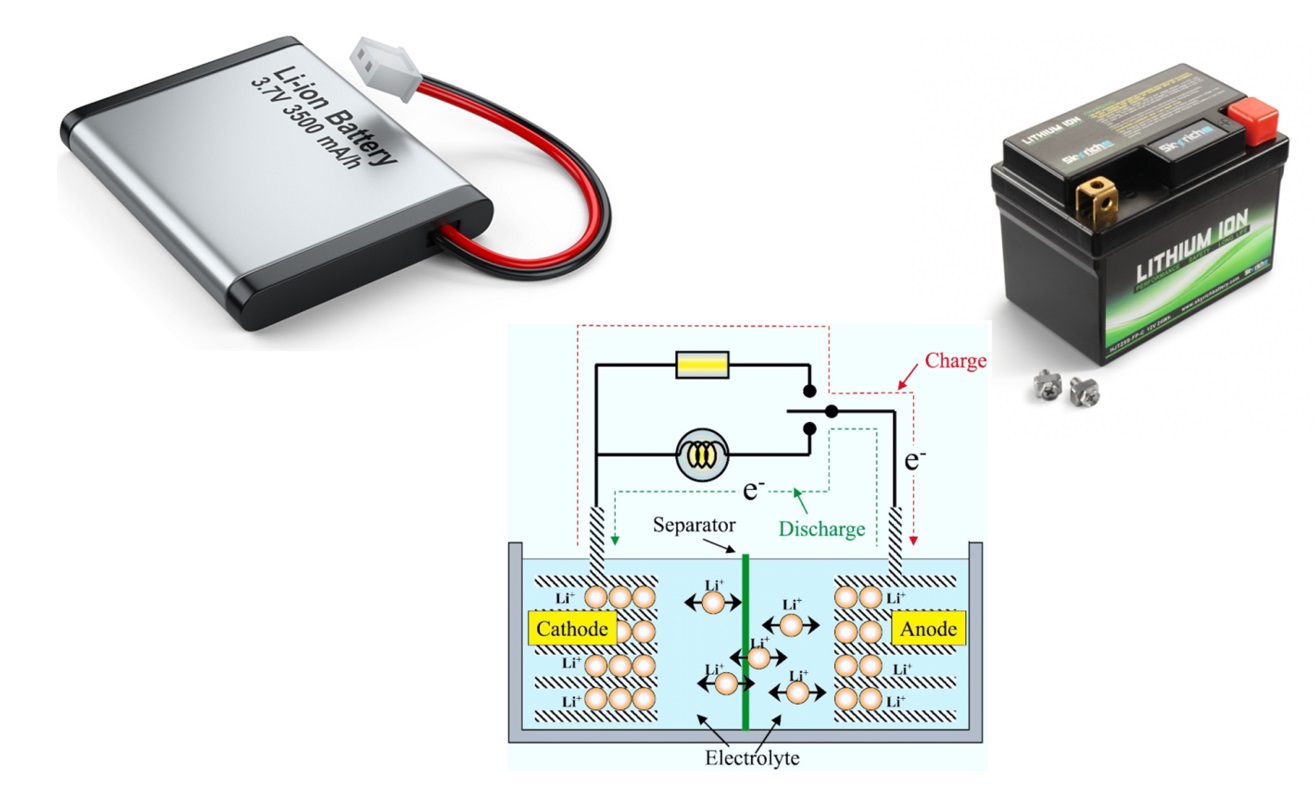
کاربرد باتری لیتیم یون:
مزایای باتری لیتیم یون:
معایب باتری لیتیم یون:
ترکیب و کیفیت ساخت باتری لیتیومی چیست؟
باتری لیتیومی مدت زمان حضور طولانی داشته اند و جزو اولین باتریهای مورد استفاده در گوشیهای هوشمند بودهاند. این باتریها از یک الکترود مثبت (اکسید کبالت لیتیوم، فسفات آهن لیتیوم یا اکسید منگنز لیتیوم (الکترود منفی) معمولا گرافیت و یک الکترولیت (کربنات اتیلن، کربنات دی اتیل) استفاده می کنند. الکترولیت در یک حلال آلی بین الکترودها ذخیره می شود.
باتریهای لیتیم پلیمری:
باتری های لیتیم پلیمر که به Li Poly یا LiPo نیز مشهورند، شبیه به باتری های لیتیم یون هستند. تفاوت اصلی باتریهای لیتوم پلیمر با لیتیم یون در نوع الکترولیت به کار رفته در آن است. در باتری لیتیم پلیمر، از پلیمرهای جامد به جای الکترولیت مایع باتریهای لیتیم یون استفاده شده است. باتری لیتیم پلیمر مشابه باتری لیتیم یون بر مبنای کاستن و افزودن یونهای لیتیمی به الکترودهای مثبت و منفی کار میکنند. باتریهای لیتیم پلیمر بسیار سبک هستند و در برابر شارژ بیش از حد و نشت مواد شیمیایی نیز مقاومتر از باتریهای لیتیم یون هستند اما تولید آنها گرانتر از باتری های لیتیم یون است و معمولا چگالی انرژی پایینتری دارند. باتری های لیتیم پلیمر بیشتر در وسایل الکترونیکی سبک وزن و گران قیمت مانند گوشیهای موبایل به کار می روند. باتری های لیتیم پلیمر به دلیل ساختاری (انواع ورقه های پلیمری) که دارند، دارای انعطافپذیری بیشتری هستند. این دسته از سلول ها با وزن کمتر، دارای ظرفیت نامی یکسان با معادل استوانهایی خود هستند که البته قیمت نهایی این نوع از باتری، بالاتر از نوع معمولی است. بصورت عامه و تجاری باتریهای لیتیم یون و لیتیم پلیمر، ویژگی های تقریبا یکسانی دارند ولی با بررسی دقیقتر می توان فهمید که به دلیل تنوع در ساختار پلیمرها، نوع پلیمری، تنوع بسیار بیشتر داررد. نوع تجاری باتریهای لیتیم پلیمر، معمولا به دلیل سبک تر بودن، جریان دهی بهتر و سیکل شارژ و دشارژ بیشتر نسبت به باتری لیتیم یون مورد استفاده قرار میگیرند و همچنین این باتری معمولا دارای جریان نشتی کمتری نسبت به نوع معادل لیتیم یون است.

انرژی:
شکل زیر، نمودار انرژی برای انواع مختلف باتری را نشان میدهد که در این نمودار، محور عمودی، چگالی انرژی را نشان میدهد و محور افقی، انرژی مخصوص(یا چگالی جرمی انرژی) را به نمایش میگذارد. کمترین انرژی مربوط به باتریهای سرب اسید است و بیشترین انرژی را نیز به باتریهای لیتیوم یون نسبت داده است. باتریهای نیکل کادمیوم(نیکاد)، از باتریهای نیکل متال هیدرید، در جایگاه پایینتری قرار دارند ولی از باتریهای سرب اسید، انرژیشان بیشتر است. سبک ترین و کم حجم ترین باتری را باتری لیتیم یون دارد و برعکس باتریهای سرب اسید، سنگینترین باتری در بین باتریهاست. شکل زیر مقایسه باتریها با معیار انرژی را نشان میدهد.
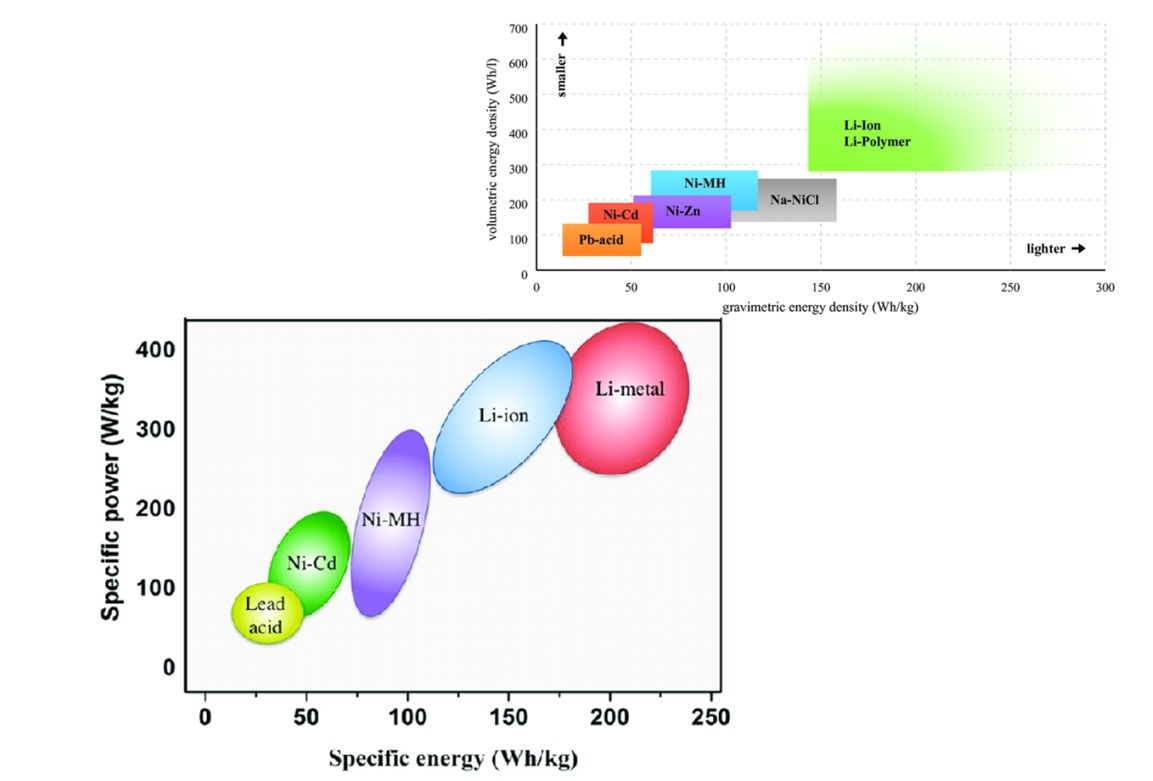
توان:
از دیگر پارامترهای مهم در باتریها، توان یک باتری است که نشان دهندهی سرعت انتقال انرژی میباشد. شکل زیر به نمودار راگون معروف است که در این نمودار، توان مخصوص(چگالی توان جرمی) و انرژی مخصوص(چگالی انرژی جرمی) دو محور این نمودار هستند و تکنولوژیهای مختلفی اعم از ابرخازنها، پیلهای سوختی و باتریها در آن مقایسه میشوند. تصویر زیر نمودار راگون و مقایسهی همزمان انرژی و توان انواع باتریها را نشان میدهد.
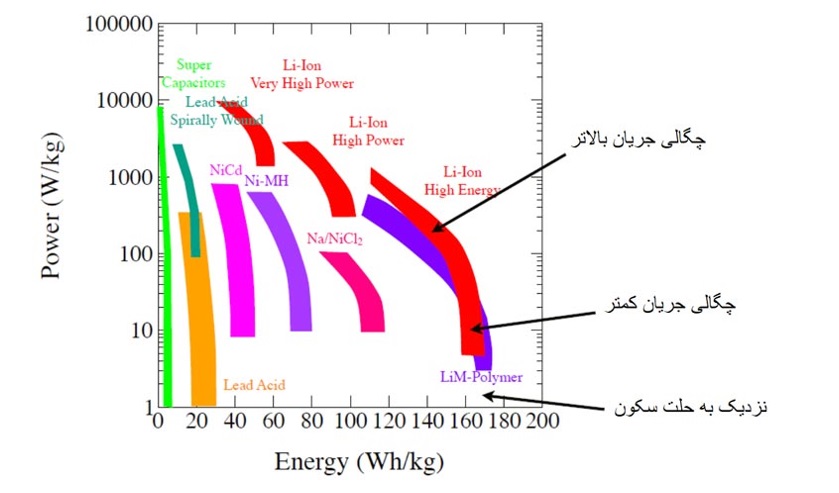
با توجه به شکل، توان در باتریهای سرب اسید، بازهای در نزدیک باتریهای نیکل کادمیوم دارند و همچنین، توان باتریهای نیکل متال هیدرید، در محودهی باتریهای نیکاد هستند. اما باتری های بسیار توان بالای لیتیم یوناند که توانی به اندازهی ابرخازن دارند و انرژی آنها نیز چند برابر یک ابرخازن است و این یک پیشرفت بسیار خوب در زمینهی باتری است. این نمودار توان باتریهای سرب اسید، نیکاد، نیکل متال هیدرید و لیتیم یون را در یک محدوده نشان میدهد. بررسی توان، برای باتریهای توان بالا حائز اهمیت است و در بقیه ی باتری ها، توان مقایسه نمی شود.
ولتاژ:
ولتاژ یک پارامتر حیاتی و لازم برای طراحی مدارات الکتریکی و الکترونیکی در باتریها است. شکل زیر به صورت بسیار ساده، ولتاژ باتریهای مختلف را با یکدیگر مقایسه کرده و ولتاژ نامی انواع باتریها را نمایش می دهد.
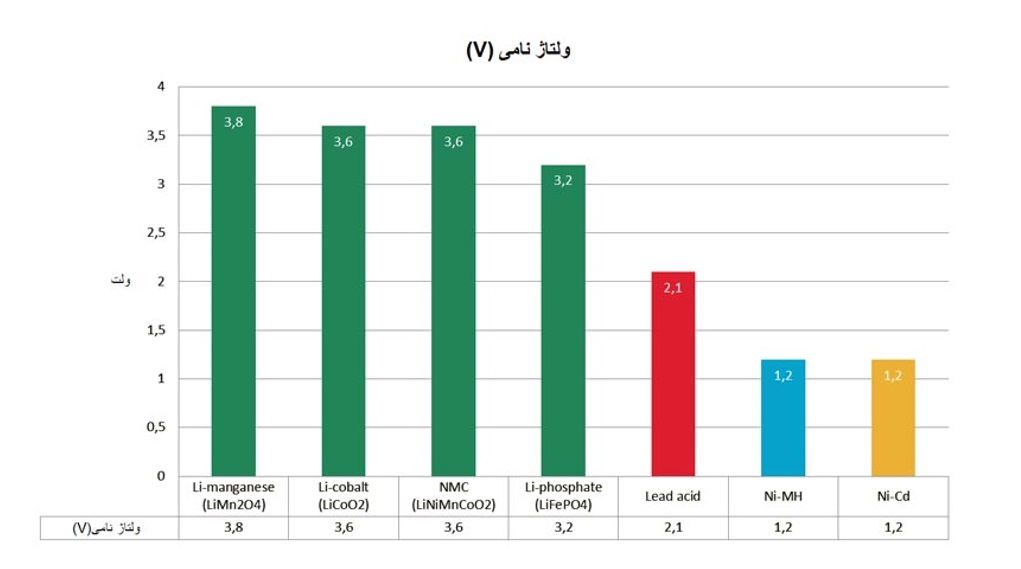
ثبات ولتاژ:
یکی دیگر از پارامترهای باتری، میزان ثابت بودن ولتاژ است. شکل زیر، نمای کلی از تغییر ولتاژ با گذشت زمان (تخلیه باتری) هر باتری را نشان می دهد. پایداری ولتاژ در انواع باتری تقریبا شبیه به هم است ولی در بازههای معین، هر باتری ممکن است از لحاظ ثابت بودن ولتاژ، از دیگر باتریها بهتر باشد. به عنوان مثال، در 20 تا 60 در صد ظرفیت دشارژ(80 تا 40 درصد ظرفیت اولیه)، باتریهای سرب اسید تقریبا ولتاژ ثابتی را از خود نشان میدهند. شکل زیر پایداری ولتاژ در انواع مختلف باتری را نشان میدهد.
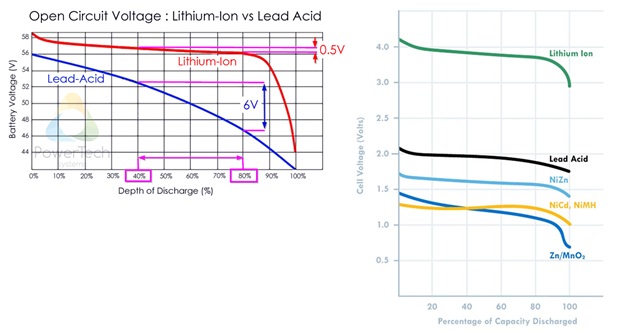
دمای کاری:
باتریهای بر پایهی نیکل، تا دماهای منفی چهل درجه توانایی کار کردن دارند و شاید در مناطق بسیار سرد، بهترین گزینه باشند. شکل زیر محدوده دمایی انواع باتریها را نشان میدهد.
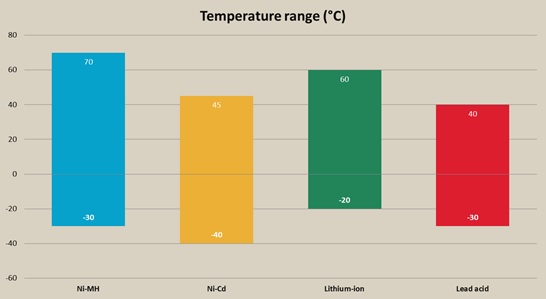
طول عمر:
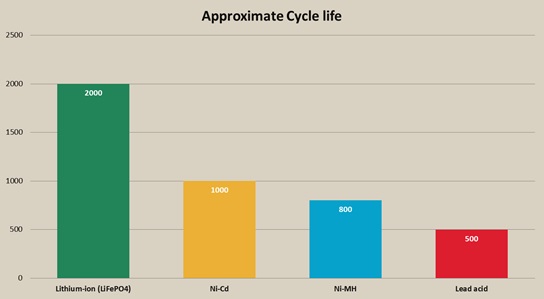
در بعضی از کاربردها، لازم است که باتری بتواند به تعداد بسیار زیادی سیکل کاری دوام آورد و اگر این طول عمر کم باشد، ممکن است هزینههای بالایی را بر ما تحمیل کند. باتریها، طول عمرهای گستردهای دارند و بسته به طراحی داخلی آنها و مواد به کار رفته در باتری، تعداد سیکل مشخصی را میتوانند سپری کنند. نمودار زیر، باتریها را بر اساس تعداد سیکل کاری دسته بندی کرده که باتریهای آهن فسفات، طول عمر بسیار خوبی را از خود به نمایش گذاشتهاند ولی به طور معمول، باتریهای لیتیم یون، طول عمر بین 500 تا 2000 سیکل کاری را از خود نشان میدهند. شکل زیر طول عمر سیکلی برای انواع مختلف باتری را نشان می دهد.
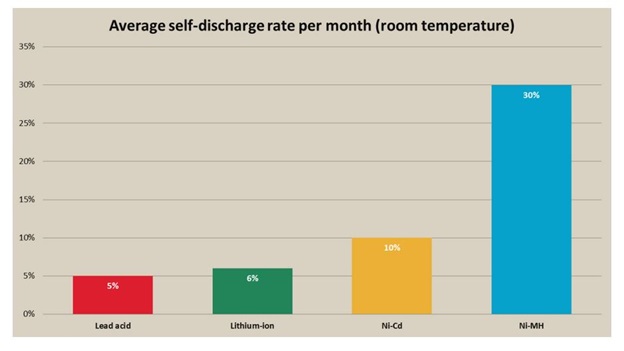
نرخ دشارژ خود به خودی:
بعضی از باتریها، بدون اینکه در مدار قرار بگیرند، انرژی خود را درون خودشان تخلیه میکنند و این پدیده، باعث میشود که ما مجبور شویم آنها را دوباره شارژ کنیم. به همین خاطر، نرخ دشارژ خود به خودی در باتریها حائز اهمیت است. باتریهای سرب اسید، نرخ دشارژ پایینی دارند ولی باتریهای نیکل کادمیوم، نرخ دشارژ خود به خودی بالایی را دارا هستند که برای این باتریها یک عیب بزرگ محسوب میشود. شکل زیر، نرخ دشارژ خود به خودی را برای انواع مختلف باتری مقایسه میکند. شکل زیر نرخ دشارژ خود به خودی در باتریهای مختلف را نشان می دهد.